细胞焦亡:对抗炎症和癌症的有力工具
发表时间:2024-11-19细胞焦亡是一种溶解性和炎症性的程序性细胞死亡,通常由炎症小体触发并由 gasdermin 蛋白执行。细胞焦亡的主要特征是细胞肿胀、膜穿孔和细胞内容物释放。在正常生理学中,细胞焦亡在宿主防御病原体感染中起着关键作用。然而,过度的细胞焦亡可能导致过度和持续的炎症反应,从而导致炎症疾病的发生。作为一种免疫原性细胞死亡,细胞焦亡可以通过诱导细胞焦亡死亡和激活强烈的抗肿瘤免疫力作为一种新的癌症消除策略。这应该会为未来的发展方向提供启示,并为利用细胞焦亡作为对抗炎症疾病和癌症的有力工具提供新思路。
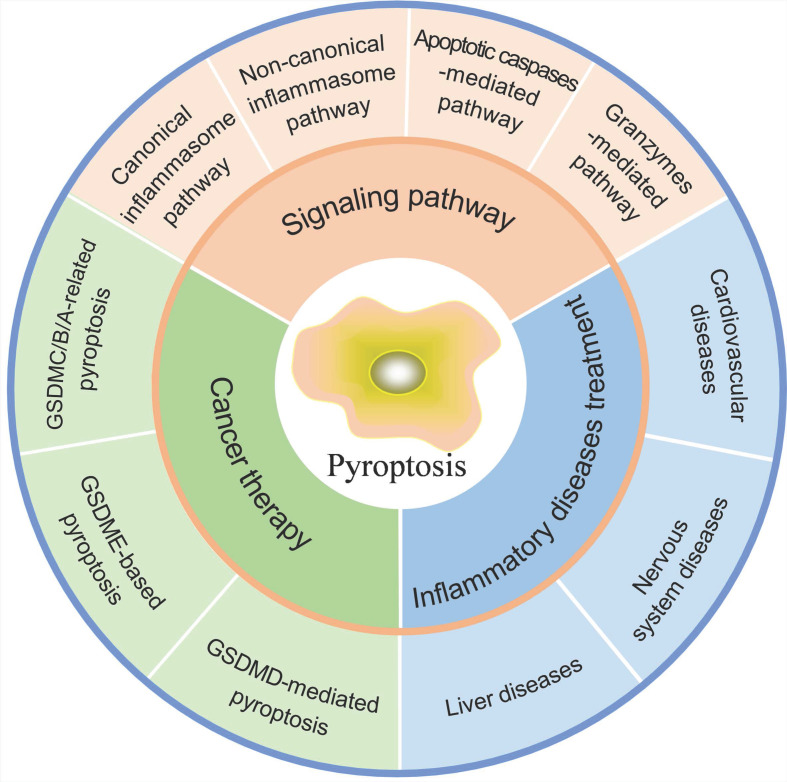
一、信号通路
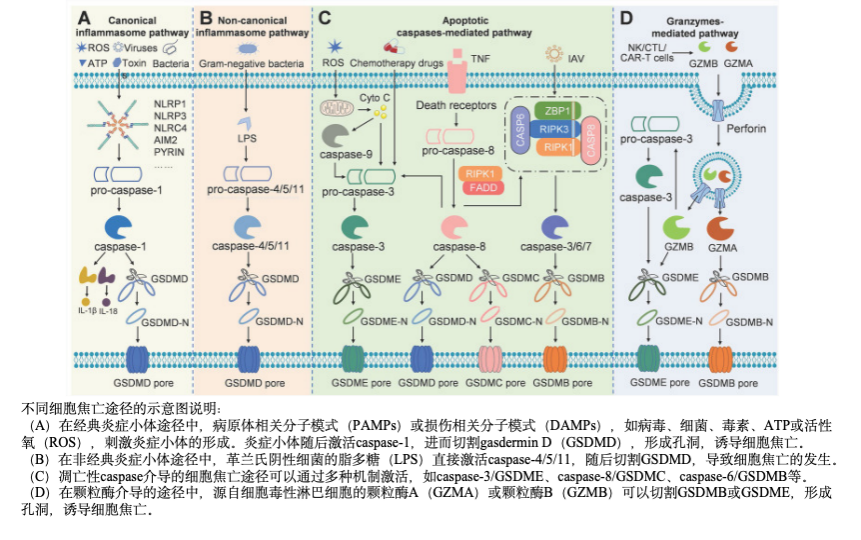
目前已鉴定出四种主要的信号通路在其诱导中发挥作用。这些通路包括经典和非经典的炎症小体通路、凋亡caspase介导的通路以及基于颗粒酶的通路。
在这些信号通路中,gasdermin蛋白充当了最终的执行者,其活性需要通过上游的caspase或颗粒酶的切割来实现。根据其功能,caspase可以分为炎症caspase和凋亡caspase。炎症caspase,如caspase-1/4/5/11主要通过诱导细胞焦亡来阻止入侵病原体的复制,并通过加工促炎细胞因子来促进其成熟和释放,从而在先天免疫反应中发挥关键作用。具体来说,caspase-1在经典的细胞焦亡途径中通过多蛋白复合物(称为炎症小体)被激活。而炎症caspase-4、-5和-11则不依赖这种复合物即可激活,它们能够直接结合脂多糖(LPS)。
另一方面,凋亡性caspase主要负责启动和执行细胞凋亡。然而,近期研究表明,这些caspase也能够作为蛋白酶切割gasdermins,进而诱导细胞焦亡。这一发现揭示了凋亡caspase在细胞焦亡中的新角色。此外,基于颗粒酶的信号通路也是细胞焦亡的一个重要途径,其具体机制尚在进一步研究中。
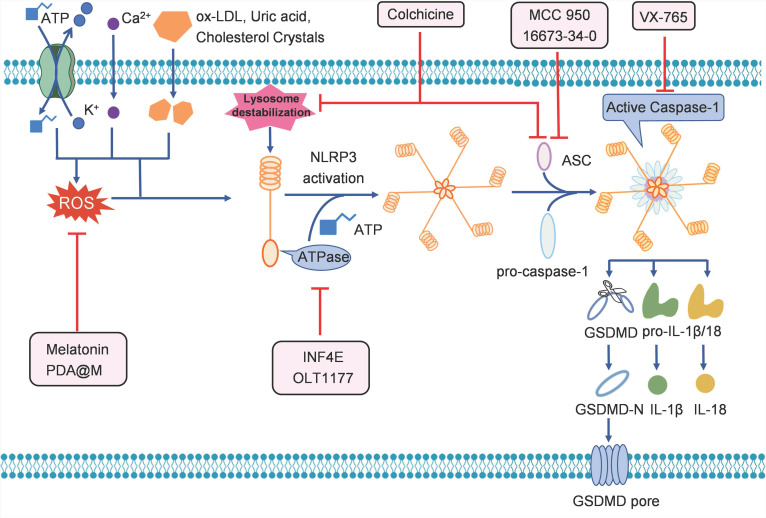
二、抑制焦亡治疗炎性疾病
在正常生理中,适度的细胞焦亡在宿主防御病原微生物中起着重要作用。然而,过度激活的细胞焦亡导致的炎症反应失调和细胞死亡可能参与许多疾病的病理进展,尤其是炎症性疾病。动脉粥样硬化的发病机制涉及平滑肌细胞增殖、内皮细胞功能障碍、促炎细胞因子分泌和细胞死亡,其中细胞焦亡在动脉粥样硬化和心血管疾病中扮演关键角色。研究发现,胆固醇晶体通过NLRP3炎症小体激活caspase-1,引发炎症反应。针对细胞焦亡的治疗策略如NLRP3炎症小体抑制剂(如INF4E、OLT1177、MCC950)和秋水仙碱,在小鼠和猪模型中可以显著减少心肌损伤和改善心脏功能,该图示为针对焦亡治疗心血管疾病的潜在策略。
三、脂质代谢信号通路
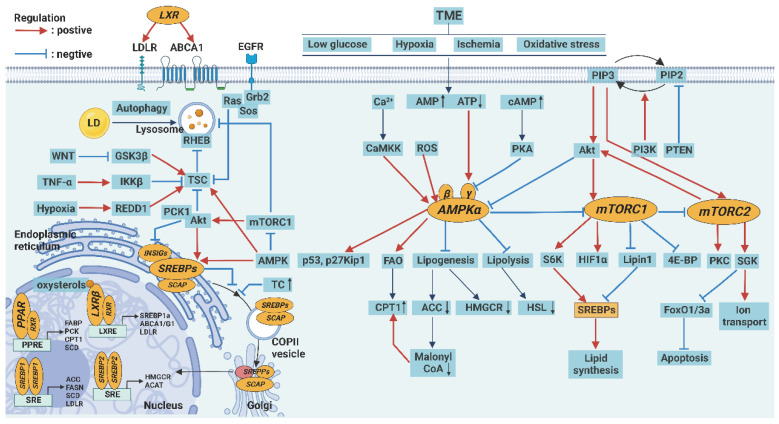
脂质代谢的关键酶的表达可以通过多种信号通路进行调控,包括AMPK、mTOR、PPAR、SREBP和LXR信号通路。在内质网中,SREBP作为非活跃前体,作为跨膜蛋白存在,并与伴侣蛋白SREBP剪切激活蛋白(SCAP)结合。当细胞内胆固醇水平降低时,SREBP被转运到高尔基体,在那里经过两步蛋白水解过程释放出N端半部分蛋白,然后成熟的SREBP转移到细胞核。在细胞核中,控制脂肪酸(FA)和胆固醇(TC)合成与转运的转录调节因子包括SREBP、LXR和PPAR,它们分别以同源二聚体或异源二聚体的形式结合在其靶基因的启动子区域的SREs、LXRE和PPREs。在肿瘤微环境(TME)中,能量应激、钙离子(Ca2+)水平升高和氧化应激增加AMP/ATP或ADP/ATP比率,激活AMPK但抑制mTOR,从而促进自噬。
肝病是危害全球人类健康的严重问题。有研究表明,细胞焦亡在肝病(如NAFLD和酒精性肝病)中发挥重要作用,主要通过NLRP3炎症小体和GSDMD-NT调节炎症和纤维化。研究发现,细胞焦亡与肝纤维化和炎症密切相关,抑制NLRP3炎症小体或其下游信号通路可以减轻肝损伤和胆管结扎诱导的肝纤维化,通过减少IL-18和IL-1β的表达,抑制中性粒细胞浸润和肝细胞死亡。治疗策略包括使用NLRP3抑制剂(如MCC950)、P2X7抑制剂、草药提取物(如水飞蓟素、二氢槲皮素)等。
为了满足科研人员需求,菲恩生物研发了一系列用于细胞焦亡及疾病检测的试剂盒,该试剂盒灵敏度高,特异性好,FineTest产品广泛应用于细胞生物学、病理学及肿瘤学研究等多种应用。

 联系我们
CONTACT
联系我们
CONTACT